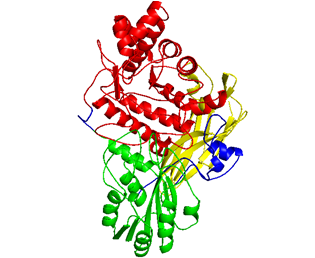
[賀端華] Chaetomella raphigera β-葡萄糖苷酶D2-BGL具有特殊蛋白結構特徵和高基質親和力,使其成為適用於水解木質纖維素生物質的高效纖維素分解酵素
發稿時間:從木質纖維素生物質中所分離的纖維素經由酵素分解獲得的可發酵糖,可將其利用於生產第二代生物燃料和其他高附加價值的化學物質。纖維素水解過程中需要三種纖維素分解酶,其中β-葡萄糖苷酶通過將纖維二糖分解為葡萄糖來完成整體酵素分解過程,因此纖維素水解的效率取決於β-葡萄糖苷酶的催化能力。本所賀端華博士的研究團隊從台灣本土真菌Chaetomella raphigera中發現β-葡萄糖苷酶D2-BGL。由酵母菌表現重組D2-BGL對纖維二糖基質親和力明顯高於商業β-葡萄糖苷酶Novozyme 188(N188)。與N188相比,使用D2-BGL可減少一半生產生質乙醇所需的時間。當與Trichoderma reesei纖維素分解酶混合使用時,它比商業纖維素分解酶混合液CTec3更有效地水解酸處理後的木質纖維素生物質。蛋白晶體結構分析發現D2-BGL屬於糖苷水解酶Glycoside Hydrolase Family 3。相對於Aspergillus 類β-葡萄糖苷酶,D2-BGL活性位點中的基質結合胺基酸F256位於一個較短的環狀結構上,此短環結構促成對纖維二糖的高基質親和力。
Link: https://biotechnologyforbiofuels.biomedcentral.com/articles/10.1186/s13068-019-1599-0